



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、普通高中课程标准实验教科书 化学1(必修)第三章第三章第一节第一节 碳的多样性碳的多样性第1页/共20页一、C、CO、CO2的转化CCO:CCO2:COCO2:CO2CO:CO2C:第2页/共20页Na2CO3与NaHCO3物理性质比较名名 称称碳酸钠碳酸钠碳酸氢钠碳酸氢钠 白色固体纯碱、苏打小苏打都溶于水,但溶解度S碳酸钠S碳酸氢钠二、Na2CO3与NaHCO3俗 名色 态水溶性第3页/共20页Na2CO3与NaHCO3的化学性质比较内容内容Na2CO3NaHCO3H+NaOHCa(OH)2CaCl2加热加热CO32-+H+=HCO3- 或CO32- +2H+=CO2+H2OHCO3-+OH
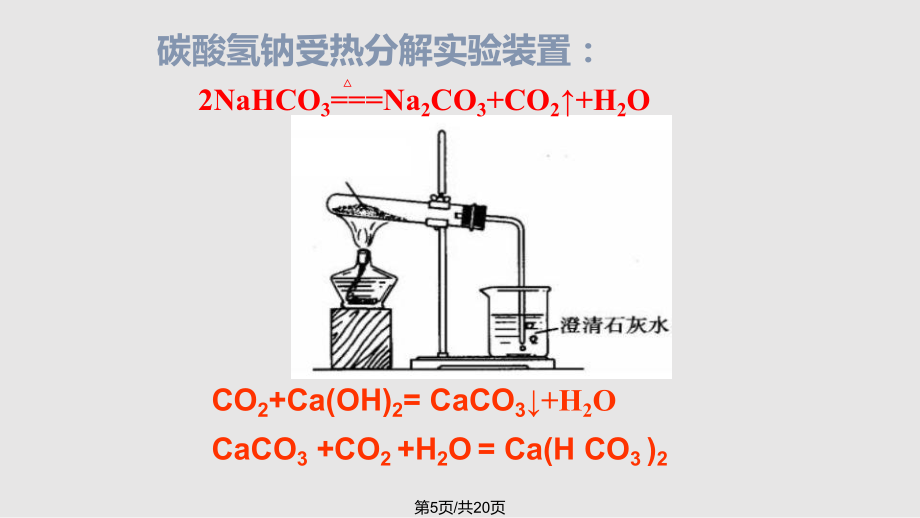
2、-= CO32- +H2OCa2+ +HCO3-+OH- = CaCO3+H2O或Ca2+ +2HCO3-+2OH- = CaCO3+ CO32- + H2O2NaHCO3=Na2CO3+CO2+H2O不反应HCO3-+H+= CO2+H2OCO32-+Ca2+= Ca CO3CO32-+Ca2+= Ca CO3不反应不反应第4页/共20页2NaHCO3=Na2CO3+CO2+H2O碳酸氢钠受热分解实验装置:CO2+Ca(OH)2= CaCO3+H2OCaCO3 +CO2 +H2O = Ca(H CO3 )2第5页/共20页溶洞中的 石花、石笋、钟乳美丽的美丽的珊瑚珊瑚天然气的燃烧燃烧第6页/
3、共20页目标引领目标引领1、掌握碳酸钠、碳酸氢钠的鉴定和除杂方法。2、了解CO2、碳酸盐、碳酸氢盐之间的转化,从而进一步了解它们的性质。 3、从定性和定量的角度理解CO2与碱反应的原理及产物确定。第7页/共20页自学探究自学探究1、如何鉴别Na2CO3固体与NaHCO3固体? 如何鉴别Na2CO3溶液与NaHCO3溶液?2 、除杂方法: Na2CO3固体中混有少量NaHCO3。 NaHCO3 固体中混有少量Na2CO3。 Na2CO3溶液中混有少量NaHCO3。 NaHCO3溶液中混有少量Na2CO3 。 3、如何实现Na2CO3与NaHCO3的相互转化? 第8页/共20页自学探究自学探究1、
4、如何鉴别Na2CO3固体与NaHCO3固体? 如何鉴别Na2CO3溶液与NaHCO3溶液?加热法加热法CaClCaCl2 2溶液溶液第9页/共20页自学探究自学探究2 、除杂方法: Na2CO3固体中混有少量NaHCO3。 NaHCO3 固体中混有少量Na2CO3。 Na2CO3溶液中混有少量NaHCO3。 NaHCO3溶液中混有少量Na2CO3。加热至恒重加热至恒重通入过量的通入过量的CO2配成浊液,通入足量配成浊液,通入足量CO2后过滤、风干后过滤、风干加适量加适量NaOH溶液溶液第10页/共20页3、如何实现Na2CO3与NaHCO3的相互转化?(1)Na2CO3转变成 NaHCO3:(
5、2)NaHCO3转变成Na2CO3:Na2CO3+CO2+H2O = 2NaHCO3 2NaHCO3+NaOH = Na2CO3+H2O 2NaHCO3=Na2CO3+CO2+H2O少量酸加热碳酸盐碳酸氢盐Na2CO3+HCl= NaHCO3+ NaCl自学探究自学探究 CO2+H2O加碱第11页/共20页CO2CO32-HCO3-同步学案 第47页概括整合概括整合三、CO2、CO32-、HCO3-的相互转化第12页/共20页四、CO2与碱反应的原理及产物确定以将CO2气体通入NaOH溶液为例:合作解疑合作解疑 精讲点拨精讲点拨定性的角度定量的角度从反应物分析从生成物分析定性的角度定量的角度第
6、13页/共20页定性的角度:当CO2少量时,生成Na2CO3;从反应物分析即:随着CO2的量由少到多,溶液的溶质发生下列变化:当CO2过量时,生成NaHCO3。NaOHNaOH、Na2CO3Na2CO3Na2CO3、NaHCO3 NaHCO3第14页/共20页 假定NaOH溶液中含NaOH 2mol,通入的 CO2为xmol,请讨论x的取值与反应产物及 溶液中溶质的关系。从反应物分析定量的角度:试用数轴表示上述关系。第15页/共20页 假定NaOH溶液中含NaOH amol,通入的 CO2为bmol,请讨论a:b的取值与反应产物及 溶液中溶质的关系。从反应物分析定量的角度:试用数轴表示上述关系。第16页/共20页定性的角度:取反应后的溶液进行检验。方法:结论:从生成物分析第17页/共20页定量的角度:(1)取反应后的溶液低温蒸干得到不含结晶水的物质,称取质量。结论:从生成物分析试
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025汽车零部件购销合同示范文本
- 2025年非金属矿物制品:耐火项目合作计划书
- 2025年沼气专用发电装置项目合作计划书
- 2025医疗机构设备购货合同模板
- 2025房产评估委托合同
- 2025年新型全液压钻机项目合作计划书
- 七年级地理结业考试高考衔接型选择题(100 题)
- 2025年智能电能表及配件合作协议书
- 2025年儿童心理咨询师考试试题及答案展示
- 2025年高压自动重合器合作协议书
- 小儿吸痰法讲稿
- 医院应急调配机制
- (格式已排好)国家开放大学电大《计算机应用基础(专)》终结性考试大作业答案任务一
- 市政工程监理规划范本(完整版)
- 起重机械产品质量证明书与合格证样表剖析
- 《机电传动控制》模块化实验装置设计
- 中秋节英文PPT
- 北师大版小学数学五年级上册单元练习题全册
- 职业病危害接触史证明
- 钢材质量证明书模板
- 用款申请单模板

评论
0/150
提交评论