



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
2023年高考化学模拟预测卷(二)(全国乙卷)
化学
(考试时间:50分钟试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:
H—1C-12N-140—16Mn—55K—39Cl—35.5Fe—56Ca-40Na—23
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
7.房县黄酒,湖北省房县特产,获得中国国家地理标志产品。其工艺流程:浸米一蒸饭一凉饭一前发酵一
后发酵一压榨一澄清一杀菌一灌装。下列说法中错误的是
A.制备黄酒工艺过程涉及过滤操作
B.浸米的原料糯米主要成分为天然高分子化合物
C.可利用紫外线对黄酒进行灭菌
D.传统型黄酒的pH为3.5~4.6是由于混有大量无机酸
【答案】D
【详解】A.制备黄酒工艺过程涉及过滤操作,即压榨后过量得到澄清溶液,A正确;
B.浸米的原料糯米主要成分是淀粉,淀粉为天然高分子化合物,B正确;
C.紫外线可以杀菌消毒,因此可利用紫外线对黄酒进行灭菌,C正确;
D.传统型黄酒的pH为3.5〜4.6是由于乙醇被氧化为乙酸,D错误;
答案选D。
8.能正确表示下列反应的离子方程式是
A.NaHSOs溶液中滴入Fe(NC)3)3溶液:2Fe3++HSO;+也0=2Fe?*+SO,+3H”
+2-
B.CuSO4溶液中通入HC1,溶液变为黄绿色:[Cu(H2O)4J+4Cr[CuCI4]+4H2O
ONaO'O'
C<^^~COONa溶液中加入少量盐酸:^^>-COO-+H+—^^-COOH
D.泡沫灭火器的反应原理:A1O;+HCO;+H2O=A1(OH)3;+CO,?
【答案】B
【详解】A.NaHSO'与Fe(NC>3)3,NO;在酸性条件下的氧化性比Fe"强,所以反应为:
+
2NO;+3HSO;=NOT+3SO^+H+H2O,A错误;
B.CuSO”溶液中通入HC1,生成黄绿色的[CuCl4r离子,反应的离子方程式为:
2+2
[CU(H2O)4]+4C1[CUC14]"+4H2O,B正确;
ONa
C./H溶液中加入少量盐酸,应先反应生成酚羟基,C错误;
,+
D.泡沫灭火器的反应原理:Al+3HCO-=Al(OH),;+3CO2T,D错误;
故选Bo
9.某锂电池材料的结构如图所示,下列有关该材料说法氐城的是
〃O
「FO—CV
.\/I
LiB
/\
LFo—c、J
“
A.其中所有元素均位于元素周期表中p区
B.该结构中阴离子部分基态原子的第一电离能:F>C>O>B
C.该化合物中B原子最外层满足8电子稳定结构
D.1mol该化合物中有8moic键
【答案】C
【详解】A.根据元素基态原子核外电子最后进入的能级将元素周期表分为5个区,其中B、C、0、F元素
均位于元素周期表中p区,而Li位于s区,A错误;
B.根据同一周期从左往右元素的第一电离能呈增大趋势,HA与OA,VA与VIA反常可知,该结构中阴
离子部分基态原子的第一电离能:F>O>C>B,B错误;
C.由题干结构示意图可知,该化合物中B原子周围有4个共用电子对,故B最外层满足8电子稳定结构,
C正确;
D.已知单键均为0键,双键是1个G键和1个兀键,由题干结构示忌图可知,1mol该化合物中有9moi。
键,D错误;
故答案为:Co
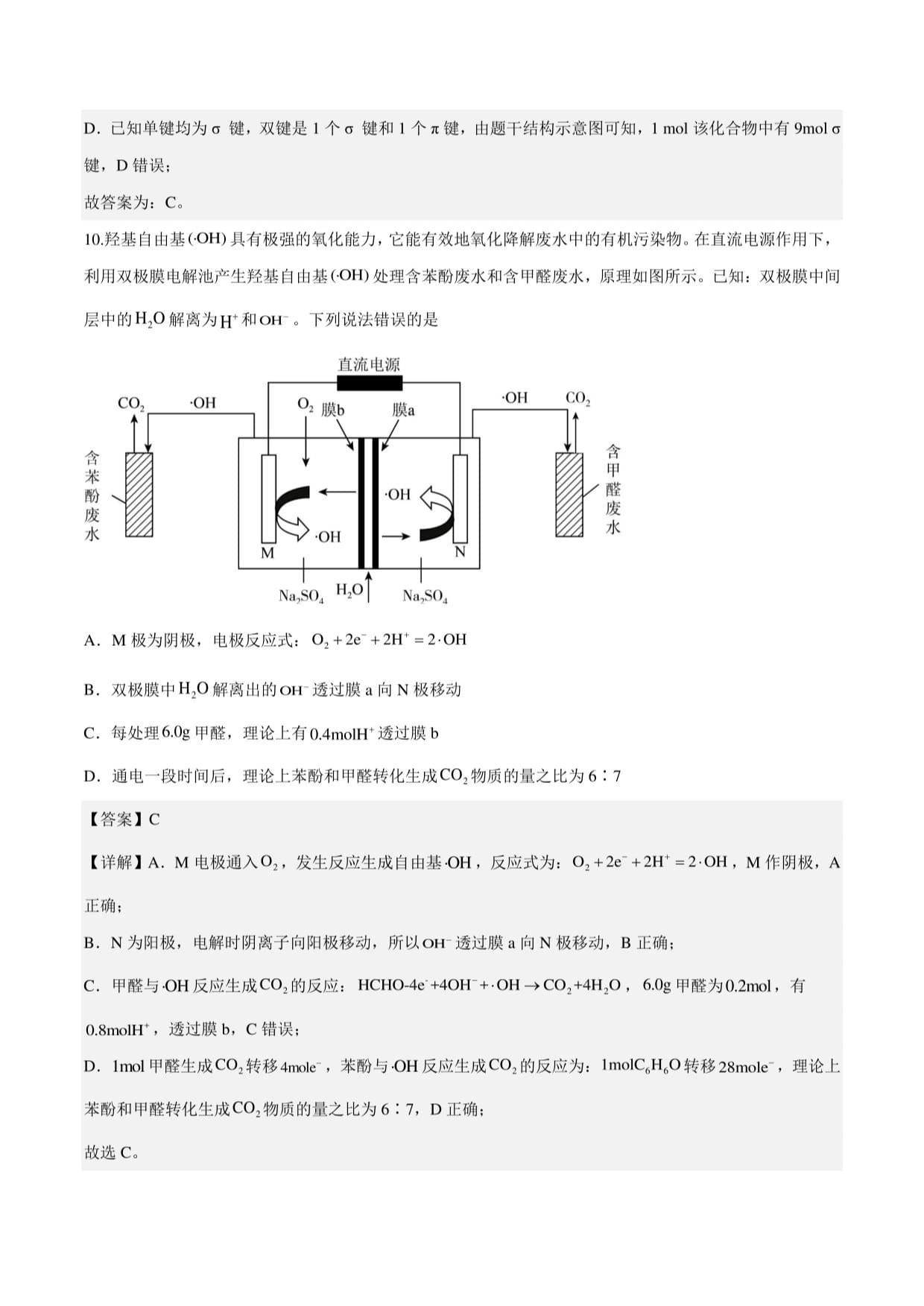
10.羟基自由基(QH)具有极强的氧化能力,它能有效地氧化降解废水中的有机污染物。在直流电源作用下,
利用双极膜电解池产生羟基自由基(QH)处理含苯酚废水和含甲醛废水,原理如图所示。已知:双极膜中间
层中的H?。解离为H+和。H。下列说法错误的是
直流电源
Na,SO」INa,SO4
+
A.M极为阴极,电极反应式:O2+2e+2H=2OH
B.双极膜中H?。解离出的OH透过膜a向N极移动
C.每处理6.0g甲醛,理论上有0.4molH+透过膜b
D.通电一段时间后,理论上苯酚和甲醛转化生成CO?物质的量之比为6:7
【答案】C
【详解】A.M电极通入发生反应生成自由基QH,反应式为:C)2+2e-+2H+=2-OH,M作阴极,A
正确:
B.N为阳极,电解时阴离子向阳极移动,所以OH透过膜a向N极移动,B正确;
C.甲醛与OH反应生成CO2的反应:HCHO-4e+4OH+OH->CO2+4H2O,6.0g甲醛为0.2mol,有
0.8molH+,透过膜b,C错误;
D.Imol甲醛生成CO,转移4mole'苯酚与OH反应生成CO?的反应为:ImolC6H6。转移28moie,理论上
苯酚和甲醛转化生成CO?物质的量之比为6:7,D正确;
故选Co
11.某溶液仅由NO;、Cl\SO:、CO;、NH:、Fe3+、A伊和K+中的若干种离子组成,且各离子浓度相等,
取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,产生无色气体;
②将①过滤、洗涤、灼烧,得到固体a;
③向上述滤液中加足量BaCb溶液,产生白色沉淀:
根据以上实验,下列推断错误的是
A.根据操作①,推断一定存在NH:
B.②中固体a为氧化铁
C.原溶液中一定不存在CO;、AF+,可能含有K+
D.说明原溶液中一定存在NO;、Cl>SO:、NH;、Fe3+、
【答案】C
【分析】加入过量的碱产生气体为NH3,溶液有NH:。信息②知加入过量的碱产生了沉淀Fe(OH)3,溶液中
有Fe3+,CO:与Fe3+会发生双水解不能共存,则溶液中不存在CO;。信息③知加溶液中有SO:。
【详解】A.由上分析溶液中一定有NH:,A项正确;
B.Fe(OH)3受热分解为氧化铁FezCh,B项正确;
C.由上分析溶液中一定有NH:和Fe3+而阴离子有SO1又溶液中各离子浓度相同,溶液中电荷不守恒,
所以一定还有和NO;。溶液中这五种离子刚好电荷守恒,所以一定不存在CO;和AF+、K+,C项错误;
D.由C项分析溶液中一定存在NH:、Fe3+、SO:、Cl^lNO3,D项正确;
故选C。
12.下列根据实验操作及现象所得出的结论正确的是
选
实验操作及现象结论
项
淀粉溶液和稀硫酸混合加热后,再加新制的Cu(OH”悬浊液加热,无砖红色沉淀
A淀粉未水解
产生
室温下,Fe(OH)3
室温下,向盛有ImLO^mobL'NaOH溶液的试管中滴加2滴O.lmoLLJMgCL溶液,
B的溶解度小于
产生白色沉淀,再滴加2滴O.lmolLFeCb溶液,又产生红褐色沉淀
Mg(0H)2
向两支试管中分别加入2mL和lmL0.1mol「Na2s2O3溶液,再向盛有ImLNa2s2O3其他条件一定时,
C溶液的试管中加入1mL蒸储水,最后同时向两支试管中加2mL0.1mol-L」H2sCU反应物浓度越大,
溶液,振荡,加入2mLNa2s2。3溶液的试管先出现浑浊反应速率越快
该环境中S02的氧
将S02通入酸性KMnO4溶液中,取反应后的溶液于试管中,再向试管中加入BaCh
D
溶液,振荡,产生白色沉淀化产物为so;
A.AB.BC.CD.D
【答案】c
【详解】A.醛基与新制氢氧化铜悬浊液反应,要求环境是碱性,题中所给信息,没有中和稀硫酸,故A
错误;
B.室温下,向盛有ImLO.2moi/LNaOH溶液的试管中滴加2滴O.lmol/LMgCb溶液,氯化镁不足,氢氧化
钠过量,再滴加氯化铁溶液,氯化铁与剩余NaOH反应生成氢氧化铁沉淀,不能比较出氢氧化铁溶解度与
氢氧化镁大小,故B错误;
C.其他条件下相同,Na2s2。3的浓度不同,因此可以探究浓度对反应速率的影响,第二支试管中,加入
2mLNa2s2O3溶液,Na2s2O3浓度比第一支试管大,第二支试管先变浑浊,说明其他条件不变,浓度越大,
反应速率越快,故C正确;
D.通入S02的酸性KMnO4溶液中,反应后溶液若是含有K2s。3,也能与BaCL产生白色沉淀,干扰实验,
故D错误;
答案为C。
13.如图为室温下某二元碱溶液中M(0H)2、M(OH)\M2+的浓度(mol-L」)对数Ige随pOH[-lgc(OH')]的变化
关系。下列说法正确的是
A.该二元碱的浓度为0.10mol/L
B.pOH=8.0时,lgc(M2+)-lgc[M(OH)+]=1.55
C.当c(M2+)=c[M(OH)+]时,pH=6.45
D.pH=7时,lgc(M2+)-lgc[M(OH)2]=8.35
【答案】B
【分析】pOH越小,溶液碱性越强,随着溶液碱性的减弱,M(OH)2浓度逐渐减小,M(OH)+浓度先增大后
减小,M2+浓度逐渐增大,因此左侧的虚线表示M(OH)2,实线表示M(OH)+,右侧虚线表示M2+。
【详解】A.根据图像可知,pOH=0时,M(OH”浓度为0.1mol/L,M(OH)+浓度为0.001mol/L,根据M守
恒可知,该二元碱的浓度大于0/mol/L,A错误;
B.根据图示可知,pOH=6.45时,c[M(OH)+]=c(M2+),此时)=c(OH)=IO"-pOH=8时,
clM(OH)]
c(M")Kin-6,45
lgc(M2+)[gc[M(OH)+]=,M(0H)+广植3=怆寸=1$5'B正确;
C.当c[M(OH)+]=c(M2+)时,pOH=6.45,此时pH=7.55,C错误;
c(M2+).c2(OH),C(M2+)10-835
D-Kad°-l9o‘c[M(OH)JW'则18C(M2+"gc[M(OH)2g示哂=lg岛丽亍,pH=7,
故lg磊;=5.65,D错误;
故答案选B。
二、非选择题:共58分,第26~28题为必考题,每个试题考生都必须作答。第35~36题为选考题,考生根
据要求作答。
(一)必考题:共43分。
O
H
S
26.二甲亚碉,(HCCH)是一种含硫有机化合物,是重要的极性非质子溶剂,能与水及许多有机溶剂
33
互溶,被誉为“万能溶剂”,有消炎止痛、镇静等作用。工业上常采用二甲硫酸与二氧化氮在60~80℃进行气
液相氧化反应制得:其装置如图(加热及夹持装置己省略)。
NaNC)2溶液
己知:①二甲硫酸是一种无色挥发性液体,由硫酸二甲酯与疏化钠反应制得:
(CH,O),SO2+Na2SfCH3SCH3+Na2SO4
②硫酸二甲酯,微棕色油状液体,遇水迅速水解成硫酸和甲醇;
③HNO?为一元弱酸,不稳定,易分解为NO和N。?。
请回答下列问题:
(1)E的名称为,D的作用是。
(2)B中的试剂可选择o
A.碱石灰B.无水CaCLC.浓硫酸D.P2O5
(3)写出HNO,的结构式o
(4)实验过程中如何确定硫酸二甲酯已完全转化为二甲硫酸_______。
(5)为了让A中较快速的产生NOz,可采取的方法是。
(6)C中生成二甲亚飒的化学方程式为。
(7)上述实验装置存在的一处错误是。
【答案】(1)恒压滴液漏斗冷凝回流
(2)BD
⑶H_O—N=O
(4)当装置中溶液由棕色变为无色即可说明硫酸二甲酯已经完全转化为二甲硫醛
(5)适当加热
O
H
S+
(6)NO2+CHtSCHs->c、HNo
H33C3
(7)缺少尾气处理装置
【分析】A装置硫酸和亚硝酸钠反应生成二氧化氮;B干燥除水;硫酸二甲酯与硫化钠反应生成二甲硫酸,
与A中产生的二氧化氮反应得到二亚甲飒。
【详解】(1)E的名称是恒压滴液漏斗,保持压强不变;D是球形冷凝管,作用是回流冷凝;
故答案为:恒压滴液漏斗;冷凝回流。
(2)B中的试剂起干燥作用,并且不能与二氧化氮反应,碱石灰可以和二氧化氮反应生成硝酸钙和亚硝酸
钙,浓硫酸中的水和二氧化氮反应生成硝酸和一氧化氮,不与无水氯化钙和五氧化二磷反应,综上所述试
剂可以选BD;
故答案为:BDo
(3)HNO2的中心原子是N原子,为+3价,形成三个共价键,每个氧原子需要成两个共价键,每个氢原子
形成一个共价键,综上所述结构式为H—0—N=0;
故答案为:H—0—N=0。
(4)硫酸二甲酯,微棕色油状液体,遇水迅速水解成硫酸和甲醇,当装置中溶液由棕色变为无色即可说明
硫酸二甲酯已经完全转化为二甲硫酸;
故答案为:当装置中溶液由棕色变为无色即可说明硫酸二甲酯已经完全转化为二甲硫醒。
(5)温度高反应速度加快,为了让A中较快速的产生N02,可以适当提高温度;
故答案为:适当加热。
O
H
S
(6)C中甲硫酸与二氧化氮反应生成二甲亚飒和一氧化氮,反应方程式为NO2+CH3SCH3-HCc、H
33
+N0;
O
H
Q
^
故答案为:NO2+CH3SCH3一HC\
3CH3
(7)甲硫醛与二氧化氮反应生成二甲亚碉和一氧化氮,尾气是一氧化氮,有毒气体需要处理,没有尾气处
理装置;
故答案为:缺少尾气处理装置。
27.钵酸锂(LiMmCU)是锂电池的正极材料,以软钵矿为原料,生产镭酸锂的流程如下:
KOH固体少量水2mol/LKOH一定量CaO
LiOH
已知:
①软镒矿的成分如下:
成分MnO?FezChCaOSiO2其他不反应杂质
质量分数69.6%7.6%5.6%9.0%8.2%
②K2M11O4在强碱性溶液(pH大于13.5)中稳定,在酸性、中性和弱碱性环境中会发生歧化反应生成MnO;和
MnO2o
③苯胺(C6H5NH2)还原性较强,在该条件下可被氧化为硝基苯(C6H5NO2)。
④铳酸锂为灰黑色粉末,离子化合物,易溶于水,难溶于无水乙醇。
(1)“氧压浸出”的浸出温度为260。。并维持500r/min的速率搅拌,此时发生的氧化还原反应的化学方程式
为。
(2)“加热溶解”和“除杂”时均要严格控制溶液pH的原因是,“除杂”中加入CaO后,需要适当加
热并搅拌的目的是,若此时溶液中c(MnO:)=2.5mol/L,则InP溶液中理论上需要加入的CaO
的质量为kg„
(3)“一系列的操作”是将所得溶液加热浓缩、冷却结晶、过滤、洗涤、干燥,其中洗涤的试剂最好选用
A.冷水B.热水C.95%的乙醇溶液D.LiOH溶液
(4)纯度的测定:取0.5800g镭酸锂[Mr(LiMmO4)=181]样品与稀硝酸和双氧水反应,将Mn元素完全转化为
Mn2+,除去过量的双氧水,调节pH,滴加指示剂,用浓度为0.3000mo1/L的EDTA标准溶液滴定,终点时
消耗EDTA标准溶液20.00mL(Mn2+与EDTA反应的化学计量数之比为1:1)
①若反应时•,N元素的化合价不变,则镭酸锂与稀硝酸和双氧水反应的离子方程式为。
②样品中锈酸锂的纯度为%(保留两位有效数字)。
【答案】(l)2MnO2+4KOH+O22K2MnO4+2H2O
(2)防止锌酸钾在酸性、中性和弱碱性环境中发生歧化反应加快反应速率,使CaSiCh颗粒增大便
于过滤8.75
⑶C
2
(4)2Mn2O4+3H2O,+10H'=4Mn"+3O,T+8H,O94
【分析】软镒矿加入氢氧化钾、加水,通入氧气氧化浸出得到锌酸钾,加入氢氧化钾溶解,加入氧化钙除
去硅等杂质,过滤除去滤渣,滤液加入苯胺、氢氧化锂,处理得到镒酸锂;
【详解】(1)“氧压浸出”的浸出温度为260。。二氧化锌和氧气、氢氧化钾发生氧化还原反应生成锯酸钾和
260c
水,2MnO2+4KOH+O22K2MnO4+2H2O;
(2)己知,K2M11O4在强碱性溶液(pH大于13.5)中稳定,在酸性、中性和弱碱性环境中会发生歧化反应生
成MnO,和MnCh;“加热溶解”和“除杂”时均要严格控制溶液pH的原因是防止镭酸钾在酸性、中性和弱碱
性环境中发生歧化反应;“除杂”中加入CaO后,氧化钙和水生成氢氧化钙,氢氧化钙和硅酸根离子生成硅
酸钙沉淀,操作需要适当加热并搅拌的目的是加快反应速率,使CaSiCh颗粒增大便于过滤;
若此时溶液中c(MnOt>2.5mol/L,更力睢孟元素守恒可知n(MnOj=n(MnO:)=2.5mol/Lxl()3L=2.5xl03moi,
m(MnO2)=2.5x1O?molx87g/mol=217.5kg,根据表格数据可知,m(SiO,)=217.5kgx&^~=28.125kg、
69.6%
m(CaO)=217.5kgx/粤=17.5kg,硅元素转化为硅酸钙需要消耗氧化钙,根据元素守恒可知,
69.6%
SiO,CaSiO3CaO,则二氧化硅需要消耗氧化钙n(CaO)=n(SiOj=警等=468.75mol,
oOg/mol
m(CaO)=468.75molx56g/mol=26.25kg,贝需要在力口入氧化钙质量为26.25kg-17.5kg=8.75kg;
(3)锯酸锂为灰黑色粉末,离子化合物,易溶于水,难溶于无水乙醇。故洗涤的试剂最好选用95%的乙醇
溶液,故选C;
(4)①若反应时,N元素的化合价不变,铳元素化合价由+3.5变为+2、氧元素化合价由-1变为0,根据电
子守恒、质量守恒配平,反应为2MnQ;+3Ha+10H+=4Mn"+3O2T+8H2。;
②Mn2+与EDTA反应的化学计量数之比为1:1,结合镒元素守恒可知,样品中镒酸锂的纯度为
0.3000mol/Lx20.00x103Lx1xl81g/mol
--------------------------------2--------------xl00%=94%-
0.5800g
28.乙烯是重要的有机化学原料,工业上可利用乙烷脱氢制备乙烯。
(1)乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
可能的引发反应有关键的解离能(kJ/mol)
C2H6(g)-C2H5-(g)+H-(g)410
C2H6®T2cH3(g)368
根据表格信息,乙烷裂解引发的反应主要为
(2)经过引发的后续反应历程为(己略去链终止过程):
C2H5-(g)->C2H4(g)+H-(g)AH)
H(g)+C2H6(g)^C2H5.(g)+H2(g)AH2
①C2H4(g)+H2(g)TC2H6(g)的AH=(用含AH]和AH?的式子表示)。
②上述历程中””所代表的反应为。
(3)CH3•中的单电子不能占据杂化轨道,则CH3•中碳原子的杂化方式为
(4)乙烷裂解中主要发生的反应及其在不同温度下的平衡常数如下表:
反应HOOKBOOK1500K
I.C2H6除「C2H4+H21.618.972.0
II.C2H6峰力gc2H4+CH460.9108.7165.8
III.C2H4脩eC2H2+H20.0150.333.2
IV.C2H2皤B2C+H26.5x1071.5x106l.OxlO5
①当裂解反应达到平衡状态时,体系将会产生大量积碳。由表中数据分析,平衡时混合气体中
(填化学式)的百分含量最大,原因是o
②为提高乙烯的产率,工业生产的适宜反应条件为(填标号)。
A.高温较长的反应时间B.高温较短的反应时间
C.低温较长的反应时间D.低温较短的反应时间
③在某温度下投入xmolC2H6发生上述反应,平衡时混合体系的压强为p,其中C2H6、C2H4、CH4的物质的
量分别为mmol、nmol、rmol,未检测出C2H2。则此温度下反应I的平衡常数Kp=(以分压表
示,分压=总压x物质的量分数)。
(5)工业上制备乙烯常使用Ni-Cr-Fe合金炉,某Ni-Cr-Fe合金的晶胞结构如图所示,,表示Ni原子,
。表示Fe原子,由4个Ni原子和2个Fe原子所形成的八面体空隙中心的一半填充Cr原子(如图中
/\位置),则该合金可表示为(填化学式)。
【答案】(DC2H6(g)-2C4-(g)
(2)-(AHi+AH?)或-AHi-AH2cH3•+C2H6-C2H5+CH4
(3)sp2
(4)H2反应IV的平衡常数远大于其它反应,体系主要得到碳和氢气,其他气体含量很少B
(3x-2n-3m-2r)np
(3x-n-2m-r)m
(5)Ni2Cr3Fe2
【详解】(1)解离能越小,发生的可能性越大,所以乙烷裂解引发的反应主要为c2H6(g)f2cH3-(g),答
案为:C2H6(g)f2cH3(g);
(2)①C2H5.(g)->C2H4(g)+H.(g)AHi②H.(g)«2H6(g)-C2H5.(g)+H2(g)AH2,由盖斯定律①+②得
c2H6(g)-c2H4(g)+H?(g),所以C2H4(g)+H2(g)fC2H6(g),AH=-(AH]+AH2)或-答案为:-(AHi
+AH2)或-AHi-AH2;
②由解离能得大小可判断主要生成甲基自由基,所以甲基自由基要转化为乙基自由基才能使反应生成乙烯,
所以历程中“……”所代表的反应为CH,・+C2H6^C2H5+CH4;
(3)CH3•结构中中心原子周围有3对电子对,杂化方式为sp2,答案为:sp2;
(4)①反应IV的平衡常数远大于其它反应,体系主要得到碳和氢气,其他气体含量很少,所以平衡时混
合,气体中H2的百分含量最大,答案为:生,反应IV的平衡常数远大于其它反应,体系主要得到碳和氢
气,其他气体含量很少;
②工业生产I、II反应生成乙烯,温度升高平衡常数增大所以需要高温,又因为皿、IV会消耗乙烯所以时
间不宜过长,故选B:
③根据氢元素守恒:n(H2)=(3x-3m-2n-2r)mol,n(总)=(3x-3m-2n-2r+m+n+r)mol=(3x-2m-n-r)mol,
n(H?)n(C2H4)
一(总严n(总)P(3x_2n_3m_2r)np(3x-2n-3m-2r)np
Pn(C2H6)(3x-n-2m-r)m,口',(3x-n-2m-r)m,
n(总)P
(5)晶胞中Fe原子个数是2,Ni原子个数是8X:+4*!=2,Ni、Fe所形成的八面体空隙中心共有6个
84
(10x1+1=6),由于只填充了一半的空隙,因此该合金可表示为Ni2CnFe2。
(二)选考题:共15分。请考生在第35、36题中任选一题作答。如果多做,则按所做的第一题计。
35.【化学一一选修3:物质结构与性质】氮族元素在复合材料等领域的应用十分广泛。
(1)中科院大连化物所某研究团队开发了一种基于氮掺杂碳上的Ru单原子(Ru/NC)高稳定丙烷脱氢制丙烯催
①按电子排布,氮元素位于元素周期表____区,基态氮原子的电子占据的最高能级电子云轮廓图为
形。
②由图可知Ru/NC中存在—(填标号)。
A.金属键B.配位键C.。键D.兀键
NH
③Zz火zu中C的杂化类型为。
H一
⑵ASH3、NH3、SbH3三种氢化物的沸点依次增大,其原因是。
(3)气态时,PC15分子的空间结构为三角双锥形(如图所示),可溶于非极性溶剂CCL,其原因是
;而固态时五氯化磷不再保持三角双锥结构,其晶格中
含有[PCI4r和[PC1]离子,可溶于极性溶剂硝基苯,其原因是
(4)错酸钝是重要的光学材料,由楮、钿、氧三种元素组成。它的一种晶体属立方晶系,可表示为xGeO2-yBi2O3,
晶胞参数a=1014.5pm,密度p=9.22gcm-3,晶胞中有两个Ge原子,则xGeOz-yBioOj中x=,
y=[列出计算式,已知Mr(GeO2)=105,Mr(Bi2O3)=466,M为阿伏加德
罗常数的值]。
【答案】⑴p哑铃BCDsp、sp2
(2)NH3中氢键对沸点的影响大于AsH3中范德华力对沸点的影响,而小于Sb%中范德华力对沸点的影响
(3)气态PCk为三角双锥,分子中正负电荷中心重合,为非极性分子,根据相似相溶原理,PC15可溶于
非极性溶剂CC14固态PCk为离子型晶体,离子型晶体一般易溶于极性溶剂,所以固态PC15可溶于硝
基苯
(4)29.22x(1014.5x10"。)‘/-2x105
466
【详解】(1)①按电子排布,氮元素位于元素周期表p区,基态氮原子的电子占据的最高能级为2P能级,
电子云轮廓图为哑铃形。
②由图可知,C与周围的原子形成3根c键,N与C之间形成◎键,N原子有孤电子对,与Ru之间形成配
位键,N、C均有一个未杂化的2P轨道,互相平行,肩并肩重叠形成大兀键,故选BCD。
NH
③“Az火zu中双键C原子,价层电子对数为3,采取sp2杂化,三键C原子,价层电子对数为2,
NNF1>
H
采取sp杂化,故C的杂化类型为sp、sp2。
(2)NH3中氢键对沸点的影响大于ASH3中范德华力对沸点的影响,而小于SbH3中范德华力对沸点的影响,
故ASH3、NEL、SbFh三种氧化物的沸点依次增大。
(3)气态PCk为三角双锥,分子中正负电荷中心重合,为非极性分子,根据相似相溶原理,PC15可溶于非
极性溶剂CC14;固态PC15为离子型晶体,离子型晶体一般易溶于极性溶剂,所以固态PC15可溶于硝基苯。
2xl05+466y
>9.22g.cm,解得丫二
(4)晶胞中有两个Ge原子,则x=2,由丁,014.5x0。)
103
9.22x(1014.5xlO)NA-2x105
466
36.【化学一一选修5:有机化学基础】一种药物的关键中间体部分合成路线如下:
7CH2cH2cl°°
、CH2cH2cl厂、,>-COOCH(BOC)0>COOC,H
------------------->HN25-N2—N人人T>
(DA物质的化学名称是。
(2)反应①的反应类型为,E物质中含氧官能团的名称为
(3)反应②要加入K2co”从平衡移动角度说明其目的:。
(4)反应⑤的化学方程式为。
/CH2cH2cl
(5)HN经过水解、部分氧化可得到分子式为C4H化合物I,写出同时符合下列条件
、CH2cH2cl
的I的所有同分异构体的结构简式.(不考虑立体异构)。
①分子结构中有一个六元环;
②核磁共振氢谱显示分子中有3种氢原子。
(6)设计以甲苯和乙烯为原料制备X(HjCNT.一CHJ的合成路线
.(无机试剂任选,用流程图表示)。
【答案】(1)邻羟基苯甲醛或者2-羟基苯甲醛
(2)取代反应酯基、酸键
(3)K2c03可与生成的HC1反应,使反应②向正反应方向移动
八V。、,CH2cH2cl八
⑷H2NQOCOOG&+HN、CH刖-HN2N-Q>C00CA+2HC,
Fe
(6)CH2=CH2—CICH2CH2CI,
rr^pOCH2COOC2H5
【分析】由题干流程图中有机物O,NU-CHO,B的分子式和B到该有机物的转化条件可知,B
的结构简式为:,由B的结构简式和A的分子式可知,A的结构简式为:
由E的结构筒式和D的分子式并结合D到E的转化条件可知,D的结构简式为:COOC2H5,
由D的结构简式和C的分子式并结合C到D的转化条件可知,C的结构简式为:o,N_[Q]^J^COOC2H5.
(5)化学式为C4H9O2N的化合物I,I的同分异构体满足①分子结构中有一个六元环,该六元环可能由4
个碳原子和一个O一个H构成,也可能由三个碳原子和三个杂原子构成;②咱-NMR谱显示分子中有3种
氢原子,可知该结构必须为对称
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 少儿古筝入门演奏指导协议
- 上海三年级数学专项训练卷2025年
- 《英语演讲》课件-Appreciation Analysis
- 2025年云南文山州广南润泽高中招聘考试真题
- 2025年娄底市卫生健康委员会市直医疗卫生单位招聘考试真题
- 2025年崇左凭祥市产业投资有限公司招聘真题
- 2026年防城港市车辆管理系统事业单位人员招聘考试备考试题及答案详解
- 2026年保定市信访系统事业单位人员招聘考试备考试题及答案详解
- 2026年巴彦淖尔市市场监督管理系统事业单位人员招聘考试备考试题及答案详解
- 2026内蒙古电影集团有限责任公司招聘15人笔试备考试题及答案解析
- 制造执行系统(MES)实施方案
- 上级转移支付管理办法
- GB/T 45953-2025供应链安全管理体系规范
- 后勤管理内控知识培训课件
- 洛阳二外小升初数学试卷
- 元明对新疆的治理
- 四川省成都市2025年中考英语试题及答案
- 知道智慧树国际金融(南开大学)满分测试答案
- 2024中华护理学会团体标准-注射相关感染预防与控制
- 档案劳动协议书
- 2025年德勤秋招测试题及答案大全

评论
0/150
提交评论