



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
第二单元
硫及其化合物的相互转化知识点1含硫物质之间的转化必备知识清单破含有相同价态的硫元素的物质通过非氧化还原反应实现转化,而含有不同价态的硫元素
的物质则通过氧化还原反应实现转化。完成下列反应:
①2SO2+O2
2SO3②2Na2SO3+O2
2Na2SO4③2H2SO3+O2
2H2SO4④2NaOH+SO2
Na2SO3+H2O⑤Na2SO3+H2SO4
Na2SO4+H2O+SO2↑(原理:强酸制弱酸;实验室常用70%的硫酸与Na2SO3反应制SO2)⑥SO2+H2O
H2SO3⑦SO3+H2O
H2SO4⑧2NaOH+H2SO4
Na2SO4+2H2O知识点拨
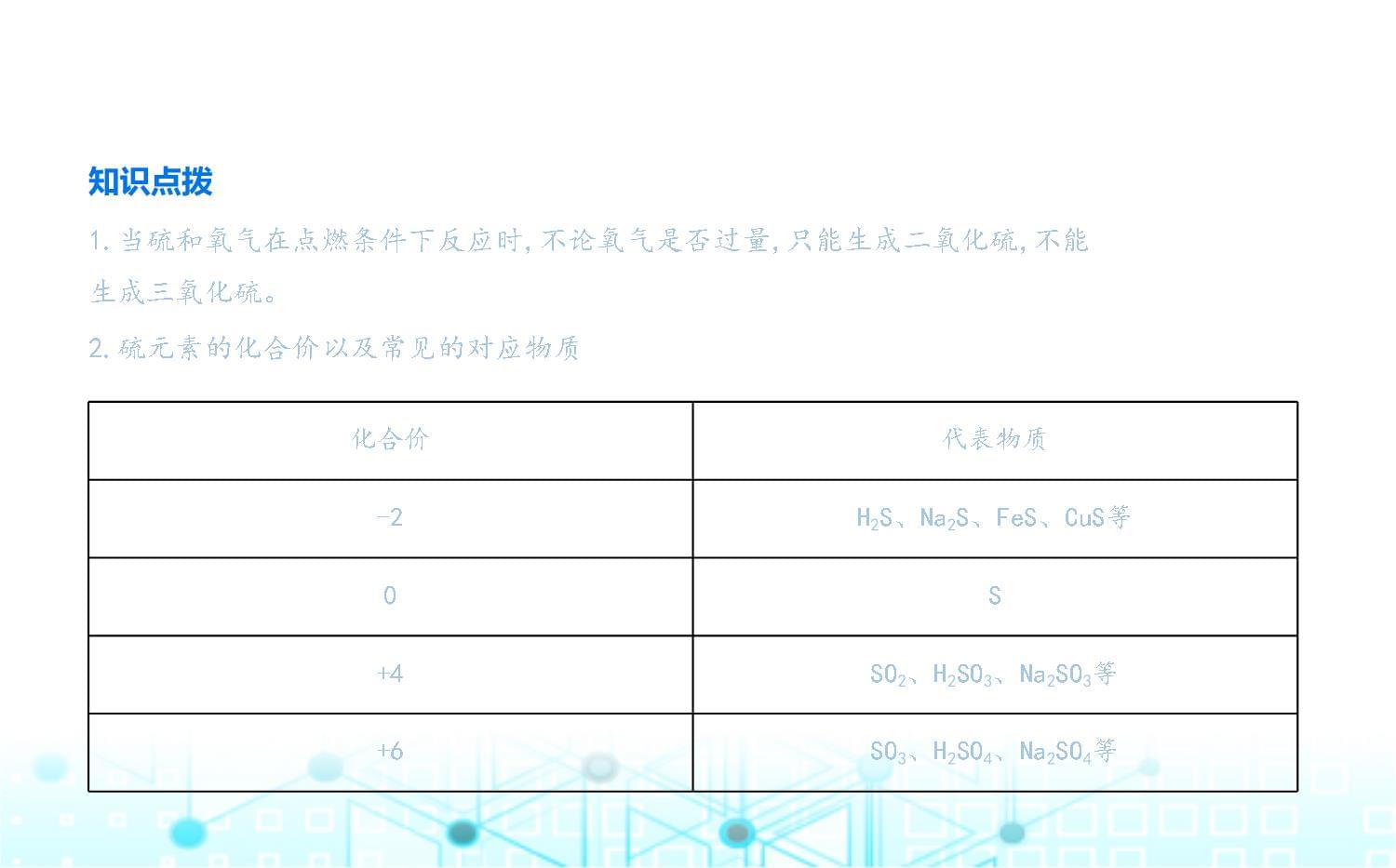
1.当硫和氧气在点燃条件下反应时,不论氧气是否过量,只能生成二氧化硫,不能
生成三氧化硫。2.硫元素的化合价以及常见的对应物质化合价代表物质-2H2S、Na2S、FeS、CuS等0S+4SO2、H2SO3、Na2SO3等+6SO3、H2SO4、Na2SO4等
知识点2氧化还原反应方程式的配平方法技巧
确定正确的最小公倍数是配平氧化还原反应方程式的关键,最小公倍数决定了氧
化还原反应中电子转移的总数。知识辨析1.硫在足量O2中燃烧,可以生成SO3。这种说法对吗?2.试管内壁的硫单质,可以用水清洗。这种说法对吗?3.SO2有还原性,浓H2SO4不可以干燥SO2气体。这种说法对吗?4.+4价的硫只能被还原。这种说法对吗?一语破的1.不对。只生成SO2,与O2的量无关。2.不对。用CS2清洗,因为硫单质易溶于CS2,难溶于水。3.不对。可以用浓H2SO4干燥SO2,因为硫元素的相邻价态间不发生氧化还原反应。4.不对。硫元素的常见化合价有-2、0、+4和+6等,+4价的硫既可以被氧化,又可以被还原。1.利用“价—类”二维图构建含硫物质的转化关系
关键能力定点破定点1硫及其化合物的相互转化SO2
H2SO3
NaHSO3
Na2SO3(均为非氧化还原反应)3.含不同价态硫元素物质之间的转化H2
O2
O3(均为氧化还原反应)2.含相同价态硫元素物质之间的转化典例物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据硫元素的
“价—类”二维图,回答下列问题:
(1)Y的化学式为
,检验Y所用的试剂是
。SO2品红溶液(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
。(3)欲制备Na2S2O3,根据氧化还原反应规律分析,下列试剂合理的是
(填字母)。a.Na2S+Sb.Na2SO3+Sc.Na2SO3+Na2SO4d.SO2+Na2SO4
2H2SO4(浓)+Cu
CuSO4+2H2O+SO2↑
b思路点拨
先根据硫元素化合价及物质类别确定“价—类”二维图中的各物质,再根据物质
性质作答。解析
X为气态氢化物H2S,Y为SO2,W为H2SO4。(1)二氧化硫具有漂白性,可以使品红溶液褪
色,加热恢复红色,所以检验二氧化硫的试剂可以是品红溶液。(2)W的浓溶液是浓硫酸,其与
铜单质在加热条件下可以发生反应,反应的化学方程式为Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑。(3)可认为Na2S2O3中S元素的平均价态为+2价,根据氧化还原反应规律分析,反应物中
S元素化合价应分别大于+2和小于+2,a中S元素的化合价都小于+2,c、d中S元素的化合价都
大于+2,b符合题意。1.配平依据(1)原子守恒:反应前后原子的个数和种类不变。(2)得失电子守恒:氧化剂得电子总数等于还原剂失电子总数。(3)电荷守恒:对于离子反应,反应前后阴、阳离子所带电荷总数相等。2.配平步骤以Cu与浓HNO3反应为例:“一标”——正确标出反应前后价态发生变化的元素的化合价,并确定同种元素化合价
的升降数。定点2氧化还原反应方程式的配平——化合价升降法
“二等”——通过最小公倍数法使化合价升降总数相等。
“三定”——确定氧化剂、还原剂、氧化产物、还原产物的化学计量数。Cu+4HNO3(浓)——Cu(NO3)2+2NO2↑+H2O“四平”——根据原子守恒用观察法配平其他物质的化学计量数,配平后将“——”改
为“
”。Cu+4HNO3(浓)
Cu(NO3)2+2NO2↑+2H2O“五查”——检查是否符合原子守恒和得失电子守恒,若为离子反应,还要符合电荷守
恒。典例某容器中发生一个化学反应,反应体系中存在Mn2+、CO2、C2
、Mn
、H+和H2O六种粒子,在反应过程中测得C2
的个数逐渐减少,下列有关说法中正确的是(
)A.该反应的氧化剂是C2
B.反应后溶液的酸性增强C.该反应中消耗1mol还原剂时,转移2mol电子D.氧化剂与还原剂的物质的量之比为2∶3C思路点拨
先根据题干信息确定氧化剂、还原剂、氧化产物、还原产物,再结合得失电子守
恒、电荷守恒以及原子守恒配平离子方程式。解析
反应体系中存在Mn2+、CO2、C2
、Mn
、H+和H2O六种粒子,“在反应过程中测得C2
的个数逐渐减少”,说明C2
是反应物,则CO2为生成物,在该反应中反应后碳元素的化合价升高,Mn
→Mn2+,Mn的化合价降低,Mn
为反应物,Mn2+为生成物。1molC2
发生反应,失去2mol电子,1molMn
参加反应,得到5mol电子,根据电荷守恒、原子守恒、得失电子守恒,配平后的离子方程式为5C2
+2Mn
+16H+
2Mn2++10CO2↑+8H2O。反应中Mn的化
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- LY/T 1610-2025水力喷射播种机
- 深度解析(2026)《GBT 35743-2017低压开关设备和控制设备 用于信息交换的产品数据与特性》
- 深度解析(2026)《GBT 35632-2017测绘地理信息数据数字版权标识》
- 影视后期PR剪辑试卷及详解
- 出纳个人工作计划报告
- 甘肃省陇南市武都区2026年九年级下学期期中化学试题附答案
- 北京市通州区2025届高三地理一模试题【含答案】
- 资产评估师机电设备试卷及解析
- 厨师高级题库及答案
- 儿科医师诊疗规范题库及解析
- 新解读《HG-T 3811 - 2023工业溴化物试验方法》新解读
- 2024年中学教学楼设计图纸(共4篇)
- 郊区道路施工方案
- 接地装置试验(电气试验课件)
- 农贸市场物业管理经营方案
- 高中主题班会 家校携手同筑梦双向奔赴育花开 下学期高二家长会主题班会课件-高中主题班会课件
- 肿瘤病人化疗的静脉管理
- 《新闻学概论》课件第1章绪论
- 上春山二部合唱钢琴伴奏正谱
- 病原菌分离培养与鉴定
- 2022-2023年高考物理二轮复习 高考电学压轴题答题策略课件(重点难点易错点核心热点经典考点)

评论
0/150
提交评论