



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
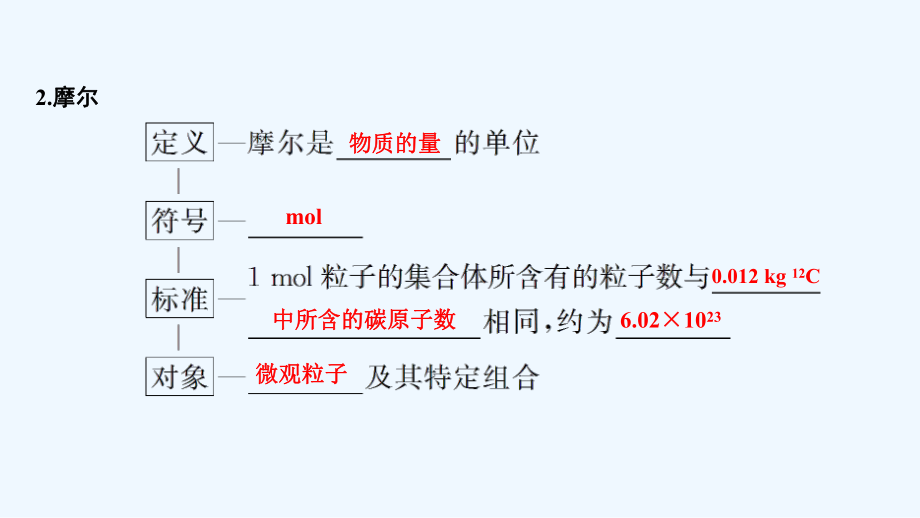
1、第二节化学计量在实验中的应用第二节化学计量在实验中的应用第第1课时物质的量的单位课时物质的量的单位摩尔摩尔学习目标学习目标核心素养建构核心素养建构1.认识物质的量的单位认识物质的量的单位摩尔。摩尔。2.认识阿伏加德罗常数,并能运用认识阿伏加德罗常数,并能运用NA进行计算。进行计算。3.理解摩尔质量的含义。理解摩尔质量的含义。一、物质的量的单位一、物质的量的单位摩尔摩尔1.物质的量物质的量(1)概念:表示含有一定数目粒子的概念:表示含有一定数目粒子的_的基本物理量。的基本物理量。(2)符号及单位:符号为符号及单位:符号为_,单位为,单位为_。 知知 识识 梳梳 理理集合体集合体n摩尔摩尔2.摩尔
2、摩尔物质的量物质的量mol0.012 kg 12C中所含的碳原子数中所含的碳原子数6.021023微观粒子微观粒子3.阿伏加德罗常数阿伏加德罗常数粒子数粒子数NA、mol16.021023【自主思考】【自主思考】1.1 mol H、1 mol H、1 mol H2的含义一样吗?为什么?的含义一样吗?为什么?提示提示意义不同,尽管都是意义不同,尽管都是1摩尔微粒,但微粒种类不同,它们分别表示摩尔微粒,但微粒种类不同,它们分别表示1摩尔氢原摩尔氢原子、子、1摩尔氢离子和摩尔氢离子和1摩尔氢分子。摩尔氢分子。二、摩尔质量二、摩尔质量Mgmol1或或g/mol相对原子质量、相对分子质量相等相对原子质量
3、、相对分子质量相等【自主思考】【自主思考】2.一种微粒的摩尔质量就是一种微粒的摩尔质量就是1 mol该微粒的质量,这种说法对吗?为什么?该微粒的质量,这种说法对吗?为什么?提示提示不对。摩尔质量的单位是不对。摩尔质量的单位是g/mol,物质的质量单位是,物质的质量单位是g,二者的意义不同。,二者的意义不同。3.已知已知1个氧原子的质量为个氧原子的质量为2.6571026 kg,请计算,请计算O2的摩尔质量为多少?与的摩尔质量为多少?与O2的相对的相对分子质量的关系是什么?分子质量的关系是什么?提示提示M(O2)2.6571023 g6.021023 mol1215.995 gmol1231.9
4、9 gmol1,氧气摩尔质量以,氧气摩尔质量以gmol1为单位,数值上与氧气相对分子质量相等。为单位,数值上与氧气相对分子质量相等。1.判断正误,正确的打判断正误,正确的打“”“”,错误的打,错误的打“”。(1)物质的量可以理解为物质的微观粒子数目。物质的量可以理解为物质的微观粒子数目。()(2)摩尔是国际单位制中七个基本物理量之一。摩尔是国际单位制中七个基本物理量之一。()(3)1 mol氧气中约含有氧气中约含有6.021023个原子。个原子。()(4)1 mol任何粒子所含有的粒子数相等。任何粒子所含有的粒子数相等。()(5)阿伏加德罗常数就是阿伏加德罗常数就是6.021023。()(6)
5、H2O的摩尔质量在数值上等于的摩尔质量在数值上等于18。()答案答案(1)(2)(3)(4)(5)(6)效效 果果 自自 测测2.下列叙述错误的是下列叙述错误的是()A.1 mol任何物质都含有约任何物质都含有约6.021023个原子个原子B.0.012 kg 12C含有约含有约6.021023个碳原子个碳原子C.在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类D.物质的量是国际单位制中七个基本物理量之一物质的量是国际单位制中七个基本物理量之一解析解析1 mol物质含有约物质含有约6.021023个微粒,但不一定为原子,个微粒,但
6、不一定为原子,A错误。错误。答案答案A3.(1)9 g H2O的物质的量为的物质的量为_,含有的氢原子数为,含有的氢原子数为_。(2)3.011023个个H2SO4分子的物质的量为分子的物质的量为_,质量为,质量为_。答案答案(1)0.5 mol6.021023(或或NA)(2)0.5 mol49 g探究一、有关四个概念的理解及摩尔质量与相对分子质量的区别探究一、有关四个概念的理解及摩尔质量与相对分子质量的区别【探究讨论】【探究讨论】1.阿伏加德罗常数的基准是什么?阿伏加德罗常数的基准是什么?提示提示以以0.012 kg 12C所含碳原子数为基准。所含碳原子数为基准。2.“1 mol小米小米”
7、,“1 mol氯氯”的说法正确吗?的说法正确吗?提示提示错误。物质的量不能表示宏观物质。错误。物质的量不能表示宏观物质。“1 mol氯氯”指代不明。指代不明。3.阴、阳离子的摩尔质量在数值上也等于其相对原子质量,对吗?阴、阳离子的摩尔质量在数值上也等于其相对原子质量,对吗?提示提示错误。阴、阳离子摩尔质量以错误。阴、阳离子摩尔质量以g/mol为单位时,数值上等于其相对原子质量。为单位时,数值上等于其相对原子质量。【点拨提升】【点拨提升】1.物质的量物质的量“四化四化”专有化专有化“物质的量物质的量”四个字是一个整体,不能拆开,也不能添字。如不能四个字是一个整体,不能拆开,也不能添字。如不能说成
8、说成“物质量物质量”或或“物质的数量物质的数量”等等微观化微观化只用来描述微观粒子,如原子、分子、离子、中子、质子、电子等只用来描述微观粒子,如原子、分子、离子、中子、质子、电子等及这些粒子的特定组合,如及这些粒子的特定组合,如NaCl;不能表示宏观的物质,如米;不能表示宏观的物质,如米具体化具体化必须指明具体粒子的种类,常用化学式表示,如必须指明具体粒子的种类,常用化学式表示,如“1 mol O”、“2 mol O2”、“1.5 mol O3”;不能说;不能说“1 mol 氧氧”集体化集体化物质的量可以表示多个微粒的特定组合或集合体,如物质的量可以表示多个微粒的特定组合或集合体,如1 mol
9、 NaCl,0.5 mol H2SO42.阿伏加德罗常数阿伏加德罗常数“三量三量”(1)基准量:基准量:0.012 kg 12C中所含的碳原子数。中所含的碳原子数。(2)准确量:是一个物理量,用准确量:是一个物理量,用NA表示,单位是表示,单位是mol1。(3)近似量:近似量:6.021023 mol1。3.摩尔质量摩尔质量“三性三性”(1)等值性:摩尔质量只是以等值性:摩尔质量只是以gmol1作单位时,在数值上与相对分子质量或相对原作单位时,在数值上与相对分子质量或相对原子质量相等。子质量相等。(2)近似性:由于电子的质量非常微小,所以离子的摩尔质量以近似性:由于电子的质量非常微小,所以离子
10、的摩尔质量以gmol1为单位时,为单位时,其数值近似等于相对分子质量或相对原子质量,如其数值近似等于相对分子质量或相对原子质量,如Na和和Na的摩尔质量都为的摩尔质量都为23 gmol1。(3)确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的量多少而改变。量多少而改变。【典题例证【典题例证1】下列叙述错误的是】下列叙述错误的是()摩尔是国际单位制中七个基本物理量之一;摩尔是国际单位制中七个基本物理量之一;1 mol任何物质都含有约任何物质都含有约6.021023个原子;个原子;6.021023就是阿伏加
11、德罗常数;就是阿伏加德罗常数;氢原子的摩尔质量是氢原子的摩尔质量是1 g;HCl的摩尔质量等于的摩尔质量等于1 mol HCl分子的质量;分子的质量;1 mol CO2中含有中含有1 mol碳和碳和2 mol氧;氧;0.012 kg 12C中含有中含有12C的数目为的数目为1 mol。A.仅仅B.仅仅C.仅仅D.全部全部解析解析中,摩尔不是物理量,是物质的量的单位;中,摩尔不是物理量,是物质的量的单位;中,物质不一定是由单个中,物质不一定是由单个原子构成的,可能是由离子或多原子构成的;原子构成的,可能是由离子或多原子构成的;中,阿伏加德罗常数为中,阿伏加德罗常数为6.021023 mol1;中
12、,中,H的摩尔质量为的摩尔质量为1 gmol1;中,摩尔质量与质量单位中,摩尔质量与质量单位不同;不同;中,中,1 mol碳和碳和2 mol氧均未指明粒子种类;氧均未指明粒子种类;中,中,0.012 kg 12C的物质的的物质的量为量为1 mol,数目为,数目为NA或约为或约为6.021023。答案答案D【学以致用【学以致用1】下列关于】下列关于“物质的量物质的量”“”“摩尔摩尔”和和“摩尔质量摩尔质量”的叙述中正确的是的叙述中正确的是()A.物质的摩尔质量等于其相对分子物质的摩尔质量等于其相对分子(原子原子)质量质量B.“物质的量物质的量”是国际单位制中的一个基本单位是国际单位制中的一个基本
13、单位C.0.012 kg 12C中所含的碳原子数为中所含的碳原子数为NA个个D.1 mol任何物质都含有约任何物质都含有约6.021023个原子个原子解析解析当物质的摩尔质量以当物质的摩尔质量以gmol1为单位时,在数值是等于其相对分子为单位时,在数值是等于其相对分子(原子原子)质质量,量,A错误;错误;“物质的量物质的量”是国际单位制中的一个基本物理量,不是单位,摩尔才是国际单位制中的一个基本物理量,不是单位,摩尔才是基本单位,是基本单位,B错误;错误;0.012 kg 12C中所含的碳原子数为阿伏加德罗常数,即中所含的碳原子数为阿伏加德罗常数,即NA个,个,C正确;正确;1 mol任何物质
14、都含有约任何物质都含有约6.021023个相应的微粒,但原子数不一定为个相应的微粒,但原子数不一定为6.021023,如,如1 mol O2含有的原子数约为含有的原子数约为26.021023个,个,D错误。错误。答案答案C探究二、物质的量、物质的质量、微粒数目之间计算关系探究二、物质的量、物质的质量、微粒数目之间计算关系【探究讨论】【探究讨论】1.3.011022个个H2O分子的物质的量是多少?分子的物质的量是多少?2.16 g O2中含有的氧原子数是多少?中含有的氧原子数是多少?【点拨提升】【点拨提升】1.质量、摩尔质量与物质的量之间的计算关系质量、摩尔质量与物质的量之间的计算关系2.摩尔质
15、量的计算方法:摩尔质量的计算方法:(1)Mm/n,该公式表示的是单位物质的量的物质所具有的质量,物质确定,其摩,该公式表示的是单位物质的量的物质所具有的质量,物质确定,其摩尔质量就确定,不能认为摩尔质量与质量成正比,与其物质的量成反比。尔质量就确定,不能认为摩尔质量与质量成正比,与其物质的量成反比。(2)Mm(一个粒子一个粒子)NA,即阿伏加德罗常数个粒子的质量。,即阿伏加德罗常数个粒子的质量。(3)Mrm(一个原子一个原子)1/12m(12C),摩尔质量在数值上等于其相对原子质量,即一,摩尔质量在数值上等于其相对原子质量,即一个原子的实际质量与一个个原子的实际质量与一个12C原子质量的原子质
16、量的1/12的比值。的比值。【典题例证【典题例证2】下列各组物质中所含氧原子的物质的量相同的是】下列各组物质中所含氧原子的物质的量相同的是()A.0.3 mol O2和和0.3 mol H2OB.6.021023个个CO2与与0.1 mol KMnO4C.0.1 mol CuSO45H2O和和0.1 mol C6H12O6D.0.1 mol H2SO4和和0.4NA个个H2O解析解析在在D项中项中0.1 mol H2SO4中含氧原子中含氧原子0.4 mol,在,在0.4NA个个H2O中氧原子也为中氧原子也为0.4 mol。答案答案D【学以致用【学以致用2】相等物质的量的】相等物质的量的CO和和
17、CO2相比较,下列有关叙述中正确的是相比较,下列有关叙述中正确的是()它们所含的分子数目之比为它们所含的分子数目之比为11它们所含的它们所含的O数目之比为数目之比为12它们所含的原子总数目之比为它们所含的原子总数目之比为23它们所含的它们所含的C数目之比为数目之比为11它们所含的电子数目之比为它们所含的电子数目之比为711A.B.C.D.答案答案D1.下列对于下列对于“摩尔摩尔”的理解正确的是的理解正确的是()A.1 mol任何物质所含有的原子数都相同任何物质所含有的原子数都相同B.摩尔是物质的量的单位,简称摩,符号为摩尔是物质的量的单位,简称摩,符号为molC.摩尔可以把物质的宏观数量与微观
18、粒子的数量联系起来摩尔可以把物质的宏观数量与微观粒子的数量联系起来D.国际上规定,国际上规定,0.012 kg C中所含有的碳原子数目为中所含有的碳原子数目为1摩摩解析解析因不同物质分子中所含有的原子个数不尽相同,所以因不同物质分子中所含有的原子个数不尽相同,所以A选项错误;物质的量选项错误;物质的量是一个物理量,摩尔是物质的量的单位,不是物理量,物质的量把宏观物质与微观是一个物理量,摩尔是物质的量的单位,不是物理量,物质的量把宏观物质与微观粒子联系起来。粒子联系起来。0.012 kg 12C中所含有的碳原子数目是阿伏加德罗常数。中所含有的碳原子数目是阿伏加德罗常数。B选项正确,选项正确,C、
19、D两项错误。两项错误。答案答案B2.下列关于摩尔质量的说法中正确的是下列关于摩尔质量的说法中正确的是()A.氢氧化钠的摩尔质量为氢氧化钠的摩尔质量为40 gB.1摩尔氧原子的质量就是氧的相对原子质量摩尔氧原子的质量就是氧的相对原子质量C.H2SO4的摩尔质量为的摩尔质量为96 gmol1D.1 mol CO2的质量以克为单位时,在数值上等于的质量以克为单位时,在数值上等于CO2的相对分子质量的相对分子质量解析解析摩尔质量的单位是摩尔质量的单位是gmol1,1 mol任何物质的质量以克为单位时,在数值上任何物质的质量以克为单位时,在数值上等于其相对分子或原子质量,等于其相对分子或原子质量,A、B
20、错误,错误,D正确;正确;H2SO4的摩尔质量为的摩尔质量为98 gmol1,C错误。错误。答案答案D3.准确理解概念内涵才能准确把握概念本质。下列有关准确理解概念内涵才能准确把握概念本质。下列有关1 mol 的含义叙述中错误的是的含义叙述中错误的是()A.1 mol任何物质都含有任何物质都含有6.021023个分子个分子B.16 g O2约含有约含有6.021023个氧原子个氧原子C.4 mol水中含有水中含有8 mol H和和4 mol OD.1 mol Ne中含有中含有6.021024个电子个电子解析解析有的物质是由分子构成的,如有的物质是由分子构成的,如CO2、O2等,而有的物质不含分
21、子,如金属等,而有的物质不含分子,如金属单质、单质、NaCl等,等,A错误;错误;16 g O2的物质的量为的物质的量为0.5 mol,所含氧原子数为,所含氧原子数为0.5 mol6.021023mol126.021023,B正确;由水的组成可知正确;由水的组成可知C正确;正确;1个个Ne中中含含10个电子,故个电子,故1 mol Ne中含中含6.021024个电子,个电子,D正确。正确。答案答案A4.0.5 mol O2中含有中含有()A.1个氧原子个氧原子B.1 mol氧分子氧分子C.NA个氧原子个氧原子D.0.5个氧分子个氧分子解析解析0.5 mol O2中含有中含有0.5 mol氧分子,氧分子数为氧分子,氧分子数为3.011023个个(0.5NA个个),含有的,含有的氧原子数为氧原子数为6.021023个个(NA个个)。答案答案C5.在在、处的横线上填上适当的内容。处的横线上填上适当的内容。解
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 2025福建厦门市湖里区招商服务有限公司招聘21人笔试参考题库附带答案详解
- 2025玉溪红塔实业有限责任公司员工招聘(29人)笔试参考题库附带答案详解
- 2025湖北鄂州市鄂城区国控投资集团下属子公司招聘17人笔试参考题库附带答案详解
- 2025浙江金华义乌市属国有企业招聘74人笔试参考题库附带答案详解
- 2026及未来5年中国1-苯基哌嗪盐酸盐市场数据分析及竞争策略研究报告
- 陕西省2025咸阳旬邑县农技推广服务人员招聘(12人)笔试历年参考题库典型考点附带答案详解
- 莱州市2025山东烟台市莱州市教育体育系统事业单位招聘37人笔试历年参考题库典型考点附带答案详解
- 河南省2025河南南阳师范学院招聘员额制硕士研究生15人笔试历年参考题库典型考点附带答案详解
- 巴中市2025四川巴中市财政投资评审中心招聘编外辅助性岗位专业技术人员1人笔试历年参考题库典型考点附带答案详解
- DB3706-T 84-2023 拥军门店等级划分与评定
- 太空舱产品买卖合同
- 《新能源发电与控制技术 第4版》 课件 第1章 新能源发电与控制技术导论
- DL-T5418-2009火电厂烟气脱硫吸收塔施工及验收规程
- 安全隐患排查及整改制度
- 人教版小学四年级信息技术上册知识点整理与归纳
- 饭店送餐合同协议书
- 《肿瘤分子生物学》课件
- 记账凭证封面直接打印模板
- 治安管理处罚法一本通
- 2023年湖南省长沙市中考物理试题(原卷)
- 头针疗法幻灯片

评论
0/150
提交评论