



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
1、一、氨基酸一、氨基酸:CH3CHCOOHCOOHNH2NH2NH2CH2CH2COOHNH2CH2CH2CH2COOH -amino acid -amino acid -amino acido-amino benzoic acidl 组成肽和蛋白质的结构单元分子组成肽和蛋白质的结构单元分子 - amino AcidHC COOHNH2R残基残基+H3NCOO-H+H2NCOO-H+H3NCOO-HCH3+H3NCOO-HCH(CH3)2+H3NCOO-HCH2+H3NCOO-HCH(CH3)CH(CH3)2CH2CH3Glycine (Gly)Alanine (Ala)Valine (Val)
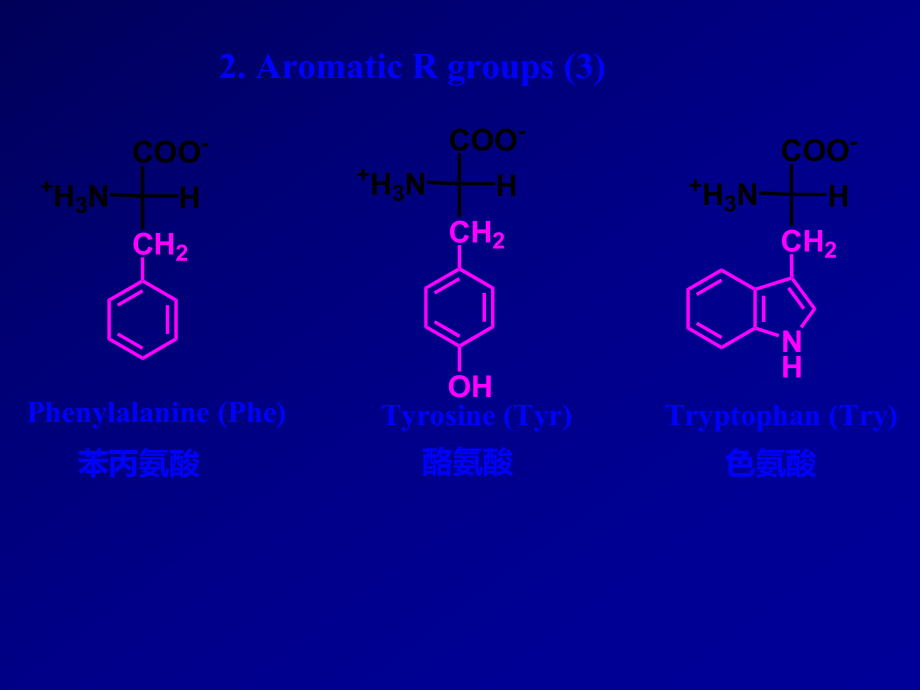
2、Leucine (Leu)Isoleucine (Ile)Proline (Pro)甘氨酸丙氨酸缬氨酸亮氨酸异亮氨酸脯氨酸1. Nonpolar, aliphalic R groups (6)+H3NCOO-HCH2+H3NCOO-HCH2+H3NCOO-HCH2Phenylalanine (Phe)Tyrosine (Tyr)Tryptophan (Try)苯丙氨酸酪氨酸色氨酸2. Aromatic R groups (3)NHOH+H3NCOO-HCH2OH+H3NCOO-HCHOH+H3NCOO-HCH2SH+H3NCOO-HCH2+H3NCOO-HCH2CH2SCH3CONH2Seri
3、ne (Ser)Threonine (Thr)Cysteine (Cys)Methionine (Met)Asparagine (Asn)Glutamine (Gln)丝氨酸苏氨酸半胱氨酸甲硫氨酸(蛋氨酸)门冬酰胺谷氨酰胺3. Polar, uncharged R groups (6)CH3+H3NCOO-HCH2CH2CONH2+H3NCOO-HCH2COO-Aspartate (Asp)Glutamate(Glu)门冬氨酸谷氨酸+H3NCOO-HCH2CH2COO-4. Negatively charged R groups (2)+H3NCOO-HCH2CH2Lysine (Lys)Ar
4、ginine (Arg)赖氨酸精氨酸+H3NCOO-HCH2CH2CH25. Positively charged R groups (3)CH2CH2NH3+NHCNH2NH2+H3NCOO-HH2CHNNHguanidinoimidazoleHistidine组氨酸(一)构型(一)构型从自然界获得的氨基酸都是从自然界获得的氨基酸都是-氨基酸;氨基酸;除甘氨酸外,除甘氨酸外,-碳原子都具有手性。碳原子都具有手性。自然界获得氨基酸基本都是自然界获得氨基酸基本都是L-L-型、型、S S型(型(L-L-半胱氨酸除外)半胱氨酸除外)COOHCH3HHOL-乳酸乳酸COOHCH3HH2NL-丙氨酸丙氨
5、酸COOHHH2NOHHCH3CHOHHOOHHCH2OHL-苏氨酸苏氨酸 D-苏阿糖苏阿糖+H3N C HCOO-R氨基酸在结晶状态或在接近中性的溶液中,是氨基酸在结晶状态或在接近中性的溶液中,是以两性离子以两性离子 (dipolar ion) 的形式存在的。是一的形式存在的。是一种内盐种内盐 (inner salt)。COOHCH3HH2N物理性质:物理性质: 高熔点固体;高熔点固体; 易溶于水,不溶于非极性溶剂。易溶于水,不溶于非极性溶剂。R C COO-NH3+HR C COO-NH2H+H+R C COO-NH3+HR C COOHNH3+H+H+ Amino acid act ei
6、ther as an acid (proton donor) Amino acid act either as an base (proton acceptor)如果在某一如果在某一pH 值下,氨基酸所带正电荷的数目值下,氨基酸所带正电荷的数目与负电荷的数目正好相等,即与负电荷的数目正好相等,即净电荷为零净电荷为零,则,则称该称该 pH 值为该氨基酸的值为该氨基酸的等电点等电点 (pI)。R C COO-NH3+HI11+R C COO-NH2HIII1Low pHHigh pHOH-H+K1R C COOHNH3+HII1OH-H+K2 等电点时,等电点时,amino acids 几乎全部以
7、两性离子几乎全部以两性离子 I 的的形式存在形式存在, 并伴以极少量、严格相等的并伴以极少量、严格相等的 II 和和 III。处于等电点的氨基酸,其溶解度最小。处于等电点的氨基酸,其溶解度最小。现在有四个氨基酸:苯丙氨酸现在有四个氨基酸:苯丙氨酸pI=5.5、脯氨酸、脯氨酸pI=6.3、门冬、门冬氨酸氨酸pI=2.8和赖氨酸和赖氨酸pI=9.7,请问在以下,请问在以下pH条件下进行电条件下进行电泳,各氨基酸的主要存在形式是什么?在外电场作用下,泳,各氨基酸的主要存在形式是什么?在外电场作用下,移向阳极还是阴极?移向阳极还是阴极? 苯丙氨酸苯丙氨酸 脯氨酸脯氨酸 门冬氨酸门冬氨酸 赖氨酸赖氨酸(
8、1)pH=7.0(2)pH=6.0(3)pH=5.0(4)pH=2.0正正 阴极阴极 正正 阴极阴极 负负 阳极阳极 正正 阴极阴极负负 阳极阳极 负负 阳极阳极 负负 阳极阳极 正正 阴极阴极正正 阴极阴极 正正 阴极阴极 正正 阴极阴极 正正 阴极阴极负负 阳极阳极 正正 阴极阴极 负负 阳极阳极 正正 阴极阴极(甲)羧基的反应(甲)羧基的反应 -氨基酸具有羧酸化学性质,可以与碱、五氨基酸具有羧酸化学性质,可以与碱、五氯化磷、氨、醇、氢化铝锂等反应。氯化磷、氨、醇、氢化铝锂等反应。RCHCOOHNH2PCl5POCl3 ,HClPhCH2OHH2ORCHCNH2ClORCHCNH2OOCH
9、2Ph活化羧基活化羧基保护羧基保护羧基(乙)、氨基的反应(乙)、氨基的反应-氨基酸还具有典型的伯胺化学性质;如氨基酸还具有典型的伯胺化学性质;如能与酸、亚硝酸、烃基化试剂、酰基化试能与酸、亚硝酸、烃基化试剂、酰基化试剂、甲醛、过氧化氢等反应。剂、甲醛、过氧化氢等反应。RCHCOOHNH2HNO2RCHCOOHOHN2HFNO2O2NFPhCH2OCOClHClRCHCOOHNHCOOCH2PhRCHCOOHNHNO2O2N脯氨酸除外OOOHOHRCCOO-NH3+HOONO-O+Ninhydrin -amino acidPurple product (or yellow for Pro)(丙)
10、、(丙)、茚三酮反应茚三酮反应 (鉴别反应)(鉴别反应)蓝或紫红色的有色物质脯氨酸除外1 1)由醛酮制备)由醛酮制备 最早发现的合成方法最早发现的合成方法CH3CHO + NH3+ HCNH2OCH3CHCNNH2H3O+CH3CHCOOHNH3(D,L)-alamine(60%)反应机理如下:反应机理如下:CRHO+NH3aldehydeH+imine- H2OCRHN HHCNCRHNHHCNCRHCNNH2 -amino nitrileH3O+CRCOOHHNH3(D,L)- -amino acid(acidic form)2 2)-卤代酸的氨化卤代酸的氨化 采用大大过量的氨采用大大过量
11、的氨邻位羧基的影响,降低了邻位羧基的影响,降低了-氨基的亲核性能氨基的亲核性能因此,反应可以得到很好地控制因此,反应可以得到很好地控制CRH2COHOcarboxylic acid(1)Br2/PBr3(2)H2OCRHCOHOBr -bromo acidNH3(大大过量)(D,L)- -amino acid(ammoniusm salt)CHCOORNH2NH43 3)Gabriel-丙二酸酯合成法丙二酸酯合成法 用这种方法可以得到其他合成方法难以得到的用这种方法可以得到其他合成方法难以得到的-氨基酸,如甲硫氨酸(蛋氨酸)氨基酸,如甲硫氨酸(蛋氨酸)CHCOOC2H5COOC2H5BrNNO
12、OKOOCHCOOEtCOOEtNOOCCOOEtCOOEtR(1)OH-(2)RXH+, H2OCCOOHCOOHRH3NCO2加热CHH3NRCOOH(L,D)- -amino acid二、多肽二、多肽二肽(二肽(dipeptide):):2 amino acid residues寡肽(寡肽(oligopeptide ):):210 amino acid residues多肽(多肽(polypeptide ):): 10 amino acid residues蛋白质(蛋白质(protein ):):molecular weight 10 Kd(一)(一)肽和肽键肽和肽键H2NCCOHHR1
13、ONHCCOOHHR2HH2NCCHR1OHNCCOOHHR2peptide bondH2O+H3NHCC NHCH2C NHCHC NHCHCNHCHCOO-OCH3OCH2CH2OOHOH2CCH(CH3)2OHSerGlyTyrAlaLeuN-terminateC-terminaten 肽链的氨基酸顺序与命名肽链的氨基酸顺序与命名(二)多(二)多肽的结构测定和端基分析肽的结构测定和端基分析纯多肽或蛋白质二硫键的拆分各条肽链选择性水解(至少两种方法)小肽段氨基酸顺序分析各肽段的氨基酸顺序(至少两组)叠加法肽链的氨基酸顺序N C SPITCNHCHHR1CONH CHR2CO+N-端氨基酸第
14、一步CHNNHSPhCHR1C NHOCHR2COHNCCHNHR1CSOPhNH CHR2COHNCH CNSR1ONHHCHPhR2COHNCHNSOPhR1+CHNh2R2CO第二步第三步PTH=苯乙内酰硫脲 (phenylthiohydrantoin)PTH-氨基酸PITC=异硫氰酸苯脂(phenyl isothiocyanate)HFH+适用于适用于50肽肽CHHNR1C NHOCHR2C NHOCHR3C OO羧肽酶断裂位点羧肽酶羧肽酶A水解断裂那些不是水解断裂那些不是Arg和和Lys的的C-端氨基酸端氨基酸羧肽酶羧肽酶B则仅水解断裂则仅水解断裂C-端为端为Arg或或Lys的氨基酸
15、的氨基酸CHHNCH2CCH2NHOSH3CCHRCO+CBrN+-S CNH3C-Br-+H2OHCH2CH2COCHNHCHNNH CHRCO+CHH3NRCO高丝氨酸内酯(homoserine lactone)CHHNCH2CCH2NHOSH3CCHRCOC NOOT-1T-2T-3T-4GASMALIKNGAAWHDFNPIDPRQCVHSDWLIACGPMTKT-2T-3placed at N-terminuspalced at C-terminusC-1C-2C-3NGAAWHDFNPIDPRGASMTKQCVHSDALIKWLIACGPMNGAAWHDFNPIDPRGASMALI
16、KWLIACGPMTKQCVHSDN-terminusC-terminusT-2T-3T-4T-1C-1C-3C-2disulfidebenzyl choroformateCH2O COCl +CHH2NCH3COOHAlaCH2OCONH CHCH3COHO+ HCl氯代甲酸苄基酯(Z-Cl)Z-Ala苄氧羰基(carbobenzoxy group),简称Cbz或ZNHCHZCH3COO+NHCHZCH3COONCHNprotontransferDCC亚胺酯(imidate)protectedactivatedCNNCNNHNHCHZCNCHNOCH3CHNH(H3C)2HCCOOO Hte
17、trahedral intermediateNHCHZCCH3ONHCHCOCH(CH3)2O+HNCHNOZ-Ala-Valdicyclohexylureanew peptide bondOCCHNH2OCH(CH3)2+.CH2ClCH2OOCCHNH-tBocCHNHR1-OOCtBocR1cold CF3COOHCH2OOCCHNH3+R1CH2OOCCHNHCOCHNH-tBocR1CHNHR2-OOCtBocR2cold CF3COOHHF Hydrolysis-OOCCHNHCOCHNHCOR1R2(From C-terminate to N-terminate)Insoluble polystyrene bead四、核苷酸四、核苷
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 排他性合作协议
- 运营隧道的养护与维修施工工艺隧道工艺标准系列之十五模板
- 婴幼儿护理技能培训课件
- 娱乐行业介绍
- 2026年工业锅炉运行培训试题及答案
- 2026年四川医疗卫生面试常见题型解析
- 2026年呼吸内科临床综合能力训练题及详细解答
- 2026年医患关系与纠纷处理能力试题含答案
- 2026年新疆油田稠油开发与处理工艺测试含答案
- 2026年股市熔断机制小测含答案
- 《药品包装用卡纸折叠纸盒》(T-CNPPA 2005-2018)
- 内蒙古呼和浩特市重点名校2025届物理高三上期末统考试题含解析
- 篮球馆硅PU施工合同
- GB/T 16288-2024塑料制品的标志
- 卡西欧图形计算器fx-9860GII SD软件说明书
- 电力工程施工组织措施
- 五年级数学上册计算题专项练习
- 人工智能赋能制造业的变革
- 腹腔镜下前列腺癌根治术护理查房课件
- 肛周脓肿的教学查房
- GB/T 11345-2023焊缝无损检测超声检测技术、检测等级和评定

评论
0/150
提交评论