



版权说明:本文档由用户提供并上传,收益归属内容提供方,若内容存在侵权,请进行举报或认领
文档简介
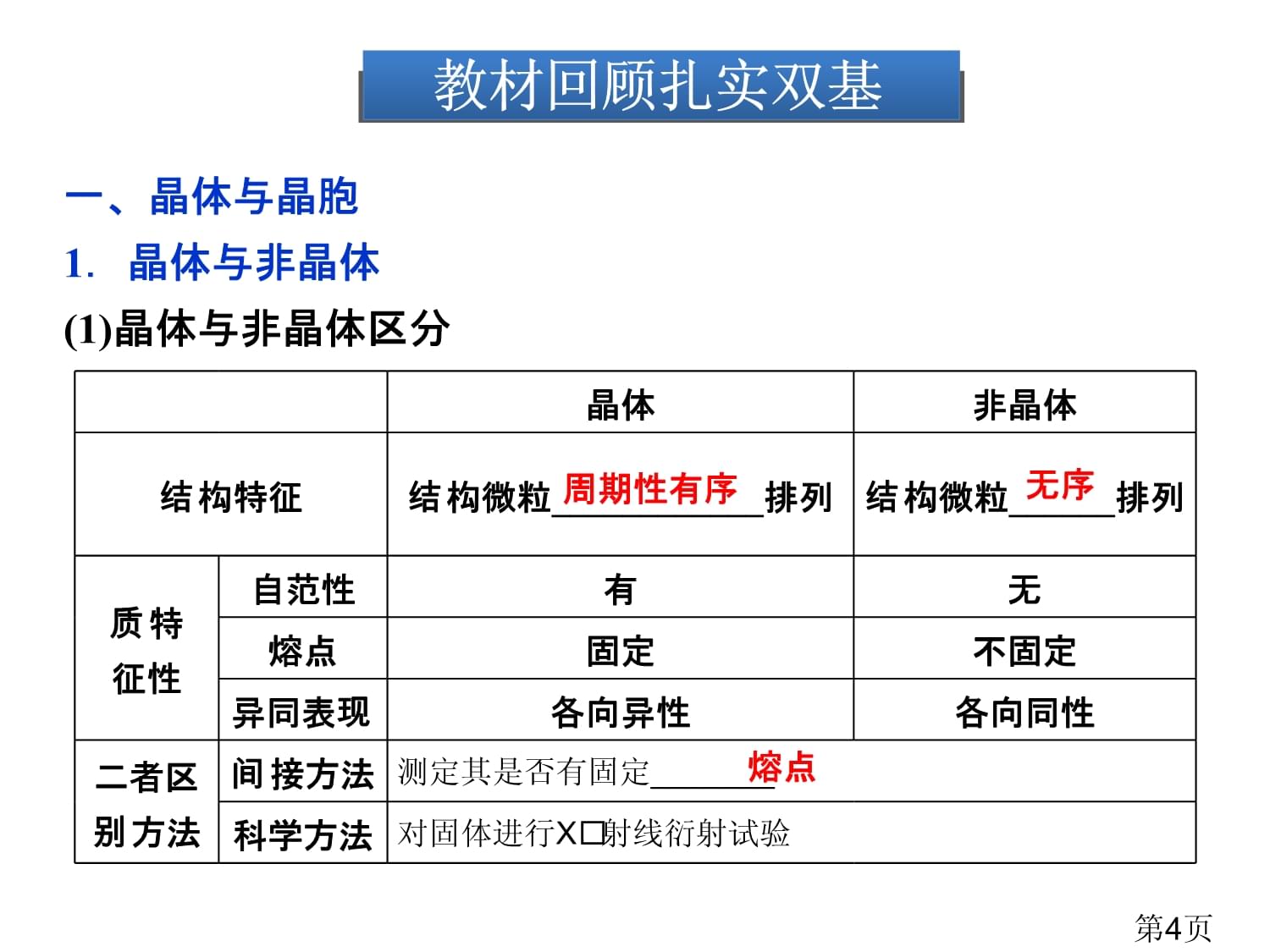
第三节晶体结构与性质第1页[考纲展示]1.了解离子键形成,能依据离子化合物结构特征解释其物理性质。2.了解原子晶体特征,能描述金刚石、二氧化硅等原子晶体结构与性质关系。3.了解金属键含义,能用金属键理论解释金属一些物理性质。4.了解分子晶体与原子晶体、离子晶体、金属晶体结构微粒、微粒间作用力区分。第2页本节目录考点串讲深度剖析知能演练高分跨栏教材回顾扎实双基第3页教材回顾扎实双基一、晶体与晶胞1.晶体与非晶体(1)晶体与非晶体区分晶体非晶体结构特征结构微粒____________排列结构微粒______排列质特征性自范性有无熔点固定不固定异同表现各向异性各向同性二者区别方法间接方法测定其是否有固定_______科学方法对固体进行X射线衍射试验周期性有序无序熔点第4页(2)取得晶体三条路径①熔融态物质凝固。②气态物质冷却不经液态直接凝固(凝华)。③溶质从溶液中析出。2.晶胞(1)晶胞:晶胞是描述晶体结构基本单元。(2)晶体与晶胞关系数量巨大晶胞“_____________”组成晶体。无隙并置第5页二、常见晶体类型结构和性质1.四种晶体类型比较类型比较分子晶体原子晶体金属晶体离子晶体组成粒子分子原子金属阳离子、自由电子阴、阳离子粒子间相互作用力___________(一些含氢键)共价键金属键离子键硬度较小很大有很大,有很小较大熔、沸点较低很高有很高,有很低较高溶解性相同相溶难溶于任何溶剂常见溶剂难溶大多易溶于水等极性溶剂范德华力第6页类型比较分子晶体原子晶体金属晶体离子晶体导电、传热性普通不导电,溶于水后有导电普通不含有导电性电和热良导体晶体不导电,水溶液或熔融态导电物质类别及举例大多数非金属单质、气态氢化物、酸、非金属氧化物(SiO2除外)、绝大多数有机物(有机盐除外)部分非金属单质(如金刚石、硅、晶体硼),部分非金属化合物(如SiC、SiO2)金属单质与合金(如Na、Al、Fe、青铜)金属氧化物(如K2O、Na2O)、强碱(如KOH、NaOH)、绝大部分盐(如NaCl)第7页2.经典晶体模型晶体晶体结构晶体详解原子晶体金刚石(1)每个碳与相邻4个碳以共价键结合,形成正四面体结构(2)键角均为109°28′(3)最小碳环由____个C组成且六原子不在同一平面内(4)每个C参加4条C—C键形成,C原子数与C—C键数之比为_______SiO2(1)每个Si与4个O以共价键结合,形成正四面体结构(2)每个正四面体占有1个Si,4个
,n(Si)∶n(O)=1∶2(3)最小环上有____个原子,即6个O,6个Si61∶212第8页晶体晶体结构晶体详解分子晶体干冰(1)8个CO2分子组成立方体且在6个面心又各占据1个CO2分子(2)每个CO2分子周围等距紧邻CO2分子有_____个离子晶体NaCl型(1)每个Na+(Cl-)周围等距且紧邻Cl-(Na+)有____个每个Na+周围等距且紧邻Na+有_____个(2)每个晶胞中含4个Na+和4个Cl-CsCl型(1)每个Cs+周围等距且紧邻Cl-有____个,每个Cs+(Cl-)周围等距且紧邻Cs+(Cl-)有_____个(2)如图为8个晶胞,每个晶胞中含1个Cs+、1个Cl-1261286第9页晶体晶体结构晶体详解金属晶体简单立方堆积经典代表Po,配位数为_____,空间利用率52%面心立方最密堆积又称为A1型或铜型,经典代表Cu、Ag、Au,配位数为_____,空间利用率74%体心立方堆积又称为A2型或钾型,经典代表Na、K、Fe,配位数为_____,空间利用率68%六方最密堆积又称为A3型或镁型,经典代表Mg、Zn、Ti,配位数为______,空间利用率74%612812第10页考点串讲深度剖析考点1晶胞组成计算方法——分割法第11页尤其提醒:(1)含有规则几何外形固体不一定是晶体,如玻璃;(2)晶胞是从晶体中“截取”出来含有代表性最小部分,而不一定是最小“平行六面体”;(3)在计算晶胞中微粒个数过程中,不是任何形状晶胞均可使用均摊法,注意分析不一样位置微粒被几个晶胞共有。第12页例1第13页【答案】(1)BaPbO3
12
(2)4第14页即时应用1.(·高考课标全国卷)ⅥA族氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出各种氧化态,含ⅥA族元素化合物在研究和生产中有许多主要用途。请回答以下问题:(1)S单质常见形式为S8,其环状结构以下列图所表示,S原子采取轨道杂化方式是______;(2)原子第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要最低能量,O、S、Se原子第一电离能由大到小次序为__________;第15页第16页(6)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛.立方ZnS晶体结构如图所表示,其晶胞边长为540.0pm,密度为________________g·cm-3(列式并计算),a位置S2-离子与b位置Zn2+离子之间距离为_______________________________________pm(列式表示)。第17页第18页(5)所给两种酸均为二元酸,当第一步电离出H+后,因为生成阴离子对正电荷有吸引作用,所以较难再电离出H+。H2SeO3中Se为+4价,而H2SeO4中Se为+6价,Se正电性更高,造成Se—O—H中O原子电子向Se原子偏移,因而在水分子作用下,也就越轻易电离出H+,即酸性越强。第19页第20页第21页考点2晶体熔、沸点高低比较方法1.不一样类型晶体熔、沸点比较(1)不一样类型晶体熔、沸点高低普通规律:原子晶体>离子晶体>分子晶体。(2)金属晶体熔、沸点差异很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。第22页第23页(3)分子晶体①分子间作用力越大,物质熔、沸点越高;含有氢键分子晶体熔、沸点反常高。如H2O>H2Te>H2Se>H2S。②组成和结构相同分子晶体,相对分子质量越大,熔、沸点越高,如SnH4>GeH4>SiH4>CH4。③组成和结构不相同物质(相对分子质量靠近),分子极性越大,其熔、沸点越高,如CO>N2,CH3OH>CH3CH3。(4)金属晶体金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高,如熔、沸点:Na<Mg<Al。第24页尤其提醒:(1)离子晶体中不一定都含有金属元素,如NH4Cl是离子晶体;金属元素和非金属元素组成晶体不一定是离子晶体,如AlCl3是分子晶体;含有金属离子晶体不一定是离子晶体,如金属晶体中含有金属离子。(2)含阴离子晶体中一定含有阳离子,但含阳离子晶体中不一定含阴离子,如金属晶体。(3)易误认为金属晶体熔点比分子晶体熔点高,其实不一定,如Na熔点为98℃,尿素熔点为132.7℃。(4)石墨属于混合型晶体,即使质地很软,但其熔点比金刚石还高,其结构中碳碳键比金刚石中碳碳键还强。第25页
现有几组物质熔点(℃)数据:据此回答以下问题:(1)由表格可知,A组熔点普遍偏高,据此回答:①A组属于________晶体,其熔化时克服粒子间作用力是________________;②硅熔点低于二氧化硅,是因为______________________;③硼晶体硬度与硅晶体相对比:_____________________。例2A组B组C组D组金刚石:3550Li:181HF:-83NaCl硅晶体:1410Na:98HCl:-115KCl硼晶体:2300K:64HBr:-89RbCl二氧化硅:1732Rb:39HI:-51MgO:2800℃第26页(2)B组晶体中存在作用力是________,其共同物理性质是________(填序号),能够用____________理论解释。①有金属光泽②导电性③导热性④延展性(3)C组中HF熔点反常是因为____________________________________________________。(4)D组晶体可能含有性质是________(填序号)。①硬度小②水溶液能导电③固体能导电④熔融状态能导电(5)D组晶体中NaCl、KCl、RbCl熔点由高到低次序为__________________,MgO晶体熔点高于三者,其原因解释为_______________________________________________。第27页【解析】
(1)A组由非金属元素组成,熔点最高,属于原子晶体,熔化时需破坏共价键。由共价键形成原子晶体中,原子半径小键长短,键能大,晶体熔、沸点高,硬度大。(2)B组都是金属,存在金属键,含有金属晶体性质,能够用“电子气理论”解释相关物理性质。(3)C组卤化氢晶体属于分子晶体,HF熔点高是因为分子之间形成氢键。(4)D组是离子化合物,熔点高,含有离子晶体性质。(5)晶格能与离子电荷数和离子半径相关,电荷越多、半径越小,晶格能越大,晶体熔点越高。第28页【答案】
(1)①原子共价键②Si—Si键能小于Si—O键能③硼晶体大于硅晶体(2)金属键①②③④电子气(3)HF分子间能形成氢键,其熔化时需要消耗能量更多(只要答出HF分子间能形成氢键即可)(4)②④
(5)NaCl>KCl>RbCl
MgO晶体为离子晶体,离子所带电荷越多,半径越小,晶格能越大,熔点越高第29页即时应用2.C和Si元素在化学中占有极其主要地位。(1)写出Si基态原子核外电子排布式_____。从电负性角度分析C、Si和O元素非金属活泼性由强至弱次序为_______。(2)SiC晶体结构与晶体硅相同,其中C原子杂化方式为________,微粒间存在作用力是________,SiC和晶体Si熔、沸点高低次序是________________。(3)氧化物MO电子总数与SiC相等,则M为______(填元素符号)。MO是优良耐高温材料,其晶体结构与NaCl晶体相同。MO熔点比CaO高,其原因是__________________,Na、M、Ca三种晶体共同物理性质是________(填序号)。①有金属光泽②导电性③导热性④延展性第30页(4)C、Si为同一主族元素,CO2和SiO2化学式相同,但结构和性质有很大不一样。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小角度分析,为何C、O原子间能形成上述π键,而Si、O原子间不能形成上述π键:_____________________________________,SiO2属于________晶体,CO2属于________晶体,所以熔点CO2________SiO2(填“<”、“=”或“>”)。(5)金刚石、晶体硅、二氧化硅、MO、CO2、M六种晶体组成微粒分别是___________________________________________________,熔化时克服微粒间作用力是___________________________________________________。第31页解析:(1)C、Si和O电负性大小次序为:O>C>Si。(2)晶体硅中一个硅原子周围与4个硅原子相连,呈正四面体结构,所以杂化方式是sp3,因为SiC键长小于SiSi,所以熔点碳化硅>晶体硅。(3)SiC电子总数是20个,则该氧化物为MgO;晶格能与所组成离子所带电荷成正比,与离子半径成反比,MgO与CaO离子电荷数相同,Mg2+半径比Ca2+小,M
温馨提示
- 1. 本站所有资源如无特殊说明,都需要本地电脑安装OFFICE2007和PDF阅读器。图纸软件为CAD,CAXA,PROE,UG,SolidWorks等.压缩文件请下载最新的WinRAR软件解压。
- 2. 本站的文档不包含任何第三方提供的附件图纸等,如果需要附件,请联系上传者。文件的所有权益归上传用户所有。
- 3. 本站RAR压缩包中若带图纸,网页内容里面会有图纸预览,若没有图纸预览就没有图纸。
- 4. 未经权益所有人同意不得将文件中的内容挪作商业或盈利用途。
- 5. 人人文库网仅提供信息存储空间,仅对用户上传内容的表现方式做保护处理,对用户上传分享的文档内容本身不做任何修改或编辑,并不能对任何下载内容负责。
- 6. 下载文件中如有侵权或不适当内容,请与我们联系,我们立即纠正。
- 7. 本站不保证下载资源的准确性、安全性和完整性, 同时也不承担用户因使用这些下载资源对自己和他人造成任何形式的伤害或损失。
最新文档
- 人工智能驱动的文言文虚词辨析教学策略研究课题报告教学研究课题报告
- 超市员工管理与处罚制度
- 副总经理助理工作流程与岗位要求
- 圆管带式输送机安装流程标准化
- 中小企业财务报销流程及审批标准
- 液压系统气蚀现象成因及维护对策
- 小学英语期末考试命题标准
- 北京市初中英语期中考试试卷库
- 小学科学课程教学计划示例
- 高中数学解析几何122条二级结论
- 5年高考数学真题分类汇编专题02常用逻辑用语(原卷版)
- 安徽2021-2025真题及答案
- JJG 1148-2022 电动汽车交流充电桩(试行)
- 向量为基,几何为本-以2025年全国新高考数学Ⅰ卷17题为例说题比赛
- 2026-2031年中国鲜冻马肉行业市场发展趋势与前景展望战略研究报告
- 军人二次召回通知书
- 曲臂车安全施工方案
- 《制氢现场氢安全管理规范》
- 防溺水事故应急预案
- 室分业务发展操作指导手册(试行)
- 水泥厂安全事故培训内容课件

评论
0/150
提交评论